Last Updated on 8. Januar 2022 by Jacek
PSMA Therapie bei Prostatakrebs
Radioliganden Therapie Lutetium-177, Actinium-225
Zielgerichtete PSMA Therapie bei fortgeschrittenem Prostatakrebs mit PSMA-617 und therapeutischem Nuklid Lutetium -177 oder Actinium -225 kann eine vielversprechende Behandlungsalternative sein.
Inhaltsverzeichnis der Seite
Voraussetzung für eine PSMA Therapie
- andere Behandlungen wie Hormontherapie, Strahlentherapie von außen oder Chemotherapie nicht mehr wirken.
- Der Tumor und die Metastasen sollen eine ausreichende Ausprägung des PSMA auf der Zelloberfläche aufweisen
- der Patient muss noch gut funktionierende Nieren- und Knochenmarksfunktion aufweisen.
Leukozyten >3000 /µl, Thrombozytenzahl > 75.000 /µl
PSMA, das Prostata-spezifische Membran Antigen, ist ein membrangebundenes Glykoprotein (Transmembranprotein) mit der Funktion eines Enzyms.
(PSMA) ist ein Transmembranprotein, das in Prostatakarzinomzellen bis zu 1.000-fach stärker exprimiert wird als in normalen Prostatazellen. „PSMA ist deshalb ein ideales Zielmolekül für die Diagnostik und zugleich auch für zielgerichtete Therapie von Prostatakrebs
PSMA kommt auf der Oberfläche gesunder Prostatazellen vor, jedoch bis zu 1.000-fach öfter auf der Oberfläche Prostatakrebs-Zellen.
Im übrigen Körper kommt das Protein kaum vor.
PRRT bedeutet Peptid-Radio-Rezeptor-Therapie, oder Peptidvermittelte Radiorezeptortherapie.
Ist eine Therapie neuroendokriner Tumore. Neuroendokrine Tumore (NET) sind häufig langsam wachsende, jedoch bösartige Tumore..
Theranostics PSMA
Der Name Theranostik besteht aus zwei Begriffen Therapie und Diagnostik.
Im englischen Sprachraum wird theranostics sehr häufig auch als personalized medicine und predictive medicine verstanden.
Das Prostata-spezifische Membran Antigen PSMA eignet sich sehr gut für die Diagnostik und für zielgerichtete Therapien von Prostatakrebs, verdient also die Bezeichnung Theranostics.
Über die Wirksamkeit und Nebenwirkungen von einer PSMA-Therapie gibt es zurzeit keine Langzeit Daten.
Wissenschaftler im Deutschen Krebsforschungszentrum entwickelten den Wirkstoff PSMA-617, der spezifisch an Prostatakrebszellen andocken kann. Der Wirkstoff lässt sich mit verschiedenen radioaktiven Substanzen markieren:
- PSMA Diagnostik: an PSMA-617 gebunden ein schwach strahlendes diagnostisches Radionuklid macht Prostatatumoren und deren Absiedlungen im PET Untersuchungen (Positronen-Emmissions-Tomographie) sichtbar, zum Beispiel PSMA-PET/CT mit Gallium-68 oder mit fluorine-18 kann selbst kleinste Ansammlungen von Prostatakrebszellen sichtbar machen.
- Tc99m-PSMA wird verwendet für die Diagnostik von Lymphknotenmetastasen während einer laparoskopischen Operation mit DaVinci Roboter und Gammasonde:
Davinci mit Gammasonde OP - PSMA-Therapie: Markiert mit einem stark strahlenden therapeutischen Radionuklid kann PSMA-617 gezielt Krebszellen vernichten. Ein erster klinischer Einsatz des Radiopharmakons im Universitätsklinikum Heidelberg verlief erfolgversprechend.
An PSMA-617 gebunden Radionuklid Lutetium-177 wird von Tumorzellen, die das Zielmolekül PSMA tragen, aufgenommen und zerstört sie von innen. Besonders für Patienten mit hormonresistenten Prostatakarzinomen, die schwierig zu behandeln sind, könnte es eine vielversprechende Behandlungsalternative sein.
Im Universitätsklinikum Heidelberg hat das Team um den Nuklearmediziner Prof. Dr. Uwe Haberkorn im Rahmen individueller Heilversuche bereits Patienten mit fortgeschrittenem Prostatakrebs mit radioaktiv markiertem PSMA-617 behandelt.
Die Ärzte setzten die therapeutischen Nuklide Lutetium -177 (ein ß-Strahler) und Actinium -225 ( ein α-Strahler).
Ein Alphastrahler wie Actinium (α-Strahler) ist ein radioaktives Nuklid, das die ionisierte Teilchen α-Strahlung aussendet. Beim radioaktiven Zerfall (Alphazerfall) werden Heliumkerne freigesetzt, bestehend aus zwei Protonen und zwei Neutronen.
Aufgrund der hohen Masse und wegen der starken Wechselwirkung mit der Materie, kann Alphastrahlung leicht abgeschirmt werden.
Durch die geringe Reichweite im Gewebe von 50-90 μm was (entspricht ca. 3-4 Zelldurchmessern) und einem hohen Energietransfer töten die α-Strahler wirkungsvoll. Das benachbarte Gewebe wird geschont.
β-Strahler mit der Reichweite von 0,6 – 4mm ist um zwei Zehnerpotenzen höher als der Durchmesser der eigentlichen Zielzelle. Das hat zur Folge, dass durch die höhere Gefahr für die Schädigung benachbarter gesunder Zellen. Die Reichweite des Beta-Strahlers Lutetium-177 beträgt im Gewebe ca. 2 mm.
Tipp: Betastrahler wie Lutetium -177 können nur bei größeren Durchmessern von Metastasen wirken.
Metastasen mit kleinerem Durchmessern wie Mikrometastasen ist besser mit dem sehr kurzstrahligen Alfastrahler Actinium -225 zu behandeln, oder noch besser: eine Kombinationstherapie von Beiden Strahler gleichzeitig.
Am 16.09.2020 hatte ich Gespräch mit einem Oberarzt von Uni-Klinikum Heidelberg, Nuklearmedizin.
Er hat mir empfohlen zuerst PSMA-Therapie mit Lutetium zu machen, erst danach eine Kombinationstherapie Lutetium + Actinium.
Am 12.11.2020 habe in Heidelberg mit PSMA Therapie mit Kombination Lutetium Lu-177 und Actinium Ac-255 angefangen.
Eine Therapie nur mit Actinium -225 machen sie wegen starken Nebenwirkungen nicht mehr.
Nach Therapie mit dem Lutetium markierten Radiopharmakon sank bei etwa 70 Prozent der Patienten der Prostatakrebsmarker PSA stark ab, nach Behandlung mit dem Actinium-markierten Radiopharmakon sankt der PSA bei allen Patienten stark ab.
In den vom Deutschen Krebsforschungszentrum in Heidelberg publizierten Daten trat ein PSA-Abfall bei 60 % der Patienten auf. Eine Subgruppenanalyse zeigte, dass viszerale Metastasen und erhöhte alkalische Phosphatase (über 220 U/l) bei Therapiebeginn signifikant mit einem schlechteren PSA-Ansprechen auf die RLT assoziiert waren.
Die PSMA-Therapie -Lutetium 177 braucht eine gewisse Mindestgröße der Metastasen um die Strahlen optimal zu nutzen (keine Mikrometastasen).
Wenn die Metastasen im PSMA-PET-CT-Bild sichtbar sind, sind das keine Mikrometastasen mehr, ist eine Wirkung der PSMA Therapie zu erwarten.
Sind die Metastasen im PSMA-PET nicht sichtbar, wird auch die Therapie vermutlich nicht wirken.
In diesem Fall wäre eine Chemotherapie sinnvoller.
Professor Wolfgang Weber von der Klinik für Nuklearmedizin am Klinikum rechts der Isar in München hat berichtet (ÄrzteZeitung vom 27.04.2021), dass von den ersten 100 mCRPC-Patienten, die die Lutetium Therapie erhielten, erreichten 40 eine PSA-Reduktion von ≥ 50 %. Bei einigen kam es sogar zu einem 100 %-igen PSA-Ansprechen, ein Drittel zeigte allerdings gar kein Ansprechen.
PSMA Lutetium Therapie PRRT
Die neue, zielgerichtete Therapie bei Patienten mit fortgeschrittenem Prostatakarzinom wird PSMA-PRRT genannt, PSMA-gerichtete Peptidrezeptor-Radionuklidtherapie.
Therapie mit an PSMA gebundenen Nuklide Lutetium-177 wird 177Lu-PSMA –PRRT genannt, eine „Bestrahlung von Innen“.
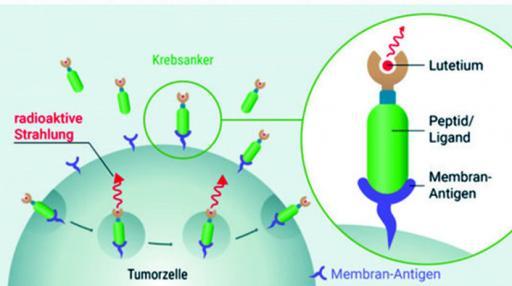
Das folgende Bild zeigt wie die PSMA-Therapie funktioniert:
Während der Infusion und auch kurz danach kommt die Therapiesubstanz, die mit Lutetium radioaktiv markiert ist, an die Tumorzelle an.
Zuerst dockt der Krebsanker an das spezifische Membran-Antigen der entarteten Zelle an. Der Tumor nimmt die radioaktive Substanz auf (Lutetium-177 oder Actinium-225).
Die Strahlung zerstört die Erbinformation (DNA) der Tumorzelle, die dann abstirbt.
Die PSMA-gerichteten Radionuklidtherapie kann die radioaktive Strahlung (ß-Strahlung) ihre therapeutische Wirkung direkt an den Tumorzellen entfalten und gleichzeitig das umgebende gesunde Gewebe schonen.
Während der Behandlung mit Lutetium lässt sich gleichzeitig im PET-Scan verfolgen, ob der Marker auch wirklich an seinem Zielort angekommen ist und ob die Dosis ausreicht.
PSMA-Therapie Kombination von Lutetium und Actinium
Neue Studie von Saarlandes Universität, Lebensverlängerung bei niedrigen Nebenwirkungen, auch wenn Lutetium alleine nicht mehr wirkt. Wirkung auf Metastasen und Mikrometastasen.
Den ganzen Text lesen Sie hier:
https://prostatakrebs-tipps.de/lutetium-actinium-psma-therapie/
Die Therapie mit Actinium hat den Vorteil einer höheren Energieabgabe und damit einer stärkeren DNA-Schädigung bei gleichzeitig kürzerer Reichweite.
Bei Alphastrahler Actinium -225 liegt die Strahlungsreichweite im Bereich 1/10 von Lutetium-177 und wirkt dadurch sehr konzentriert im Bereich der Krebszelle und verschont das umliegende Gewebe besser.
Die bisher bekannte Radionuklidtherapie mit Alpharadin, Xofigo, wird nur bei Knochenmetastasen angewendet.
Die PSMA_PRRT Therapie wirkt in ganzem Körper auf die Metastasen.
Einschlusskriterien für die PSMA Therapie
- Nicht operierbarer, mCRPC mit PSMA-positiven Metastasen in der PSMA-Bildgebung
- Lebenserwartung > 4–6 Monate
- Laufende Hormontherapie mit Unterdrückung des Testosterons in den Kastrationsbereich
- Tumorprogress
- trotz Anwendung der modernen Androgenentzugstherapien (Abiraterone und/oder Enzalutamid);
- trotz Durchführung mindestens einer Chemotherapie (Docetaxel und/oder Cabazitaxel); Ausnahme: Es besteht eine Kontraindikation zur Chemotherapie;
- trotz Anwendung einer Radium-223-Therapie; Ausnahme: Vorliegen viszeraler Metastasen oder einer sonstigen Kontraindikation zur Radium-223-Therapie
- Beschluss zur Durchführung eines individuellen Heilversuchs mit Lutetium-PSMA-RLT in einem interdisziplinären Tumorboard beziehungsweise unter Einbeziehung des primär behandelnden Urologen/Onkologen mit uroonkologischem Schwerpunkt
Tipps Ratschläge PSMA-Therapie
PSMA Lutetium Therapie wirkt am stärksten gegen Metastasen in den Lymphknoten, weniger stark gegen Knochenmetastasen, noch weniger bei Lebermetastasen
Enzalutamid kann die PSMA Expression erhöhen – und dadurch könnte die Wirkung verbessern. Es wird daran noch geforscht.
Nebenwirkungen Lutetium, PSMA Therapie
In den meisten Fällen wird die Therapie gut vertragen.
Für die Nebenwirkungen einer PSMA-Therapie gibt es zurzeit keine Langzeit Daten.
Meistens kommt es zu Nebenwirkungen wie Geschmacksstörungen und Mundtrockenheit sowie Abgeschlagenheit.
Gelegentlich kann auch zu Übelkeit kommen.
Die Mundtrockenheit kann sich durch die Schädigung von Speicheldrüsen nach jeder weiteren Infusion verstärken.
Das PSMA-bindende Radiopharmakon wird sowohl über die Nieren als auch über die Leber und Gallenblase ausgeschieden, so dass sie durch die Strahlen belastet werden. Nach mehrfacher PSMA-Therapie, nach mehreren Zyklen können sie beschädigt werden. Als Vorsorge ist eine verstärkte Flüssigkeitszufuhr erforderlich.
Die Leber- und Nierenwerte werden nach der PSMA-Therapie weiter kontrolliert. Risikoorgane sind vor allem die Speichel- und Tränendrüsen, in denen das PSMA-gerichtete Konjugat ebenfalls angereichert wird. Die Gefahr einer dauerhaften Schädigung mit Funktionsverlust (Mundtrockenheit) erscheint nach bisherigen Erkenntnissen als gering.
Wenn sich in der Knochen viele Metastasen befinden, kann diese Strahlentherapie als Langzeitwirkung auch Knochenmark schädigen, was sich auf die Blutproduktion auswirken, kann zum Beispiel zu Anämie führen.
Auch nach Jahren können sich durch die Strahlen Nebenwirkungen entwickeln, können zur Bildung von neuen Tumoren beitragen.
Die Nebenwirkungen der PSMA Therapie mit Lutetium -177 (β-Strahler) scheinen in der Praxis nicht so stark sein wie bei der Therapie mit Actinium -225 (α-Strahler).
Die Halbwertszeit von Actinium -225 dauert 10 Tage dauert, nach 5 Wochen bleibt noch ein Zehntel der ursprünglichen Aktivität.
Actinium -225 greift die Speicheldrüsen an. Man ist die ersten Wochen erst mal völlig trocken im Mund. Der Speichel soll sich scheinbar nach 2 Monaten wieder einstellen, aber eine Schädigung bleibt, besonders nach mehreren Infusionen.
Bei mir nach der zweiten Lutetium + Actinium Therapie bleibt die Mundtrockenheit dauerhaft.
Wenn der Speichel fehlt, wird alles empfindlich, die Zunge wird rau und brennt. Mit jedem Bissen muss man trinken. Ohne Speichel schmeckt alles nicht mehr. Da die schützende und reinigende Wirkung des Speichels ausbleibt, bilden sich im Mund Kolonien von Bakterien und die Zähne sind stark gefährdet.
Über Mundtrockenheit nach PSMA-Therapie, was man dagegen tun kann, habe ich hier geschrieben: mundtrockenheit-xerostomie-nach-psma-therapie/
Erfahrungen mit Lutetium Therapie
Die Entscheidung zur PSMA-Therapie wird nach Vorliegen aller Befunde gemeinsam mit dem behandelnden Urologen, Onkologen und ggf. den Experten der Therapie-durchführender Uniklinik in einem interdisziplinären Konsens getroffen.
Eigene Erfahrung, Ablauf der PSMA Therapie
Nach Durchführung der vorbereitenden Untersuchungen, wie PSMA-PET-CT, Nierenszintigraphie, Bluttest erfolgt über eine Vene
– zuerst eine Infusion mit Infusionslösung (Isotonische Kochsalzlösung 0,9%), ca. 30 Minuten,
– dann die Infusion der PSMA-Radionuklidsubstanz, nur ein paar Minuten,
– danach erneut mit Infusionslösung, ca. 4 Stunden.
Kurz vor, während und nach der Lutetium-177 Infusion habe ich meine Speicheldrüsen mit Kühlbeutel gekühlt, um die Nebenwirkungen zu mildern.
Die Dauer des stationären Aufenthalts beträgt wenige Tage, wobei täglich erfolgte eine Untersuchung unter einem Gamma-Scanner und ein mal eine Ganzkörper-Schichtuntersuchung (wie CT), um die Verbreitung von Lutetium-177 in Metastasen zu prüfen.
Ich war 4 Tage in der Strahlenquarantäne, dann durfte ich wieder nach Hause.
In Abhängigkeit der Untersuchungsergebnisse sowie des Allgemeinbefindens werden in der Regel zwei Zyklen der PSMA-Therapie mit Abstand von 2 Monate durchgeführt. Ca. 6 Wochen danach erfolgt eine PSMA-PET-CT Kontrolluntersuchung.
Bei Bedarf und abhängig von Gesundheitszustand ist es möglich weitere Zyklen PSMA Therapie durchzuführen, meistens sind das insgesamt 4 Zyklen.
! Ich habe meine Lutetium-177 PSMA-Therapie in Stuttgart in Katharinenhospital gehabt.
Ich kann das Krankenhaus mit der Abteilung Nuklearmedizin weiter empfehlen.
Die Erfahrungen verschiedenen Kliniken zeigen, dass die PSMA-Therapie mit radioaktiven Nuklid 177-Lutetium gut verträglich ist und weit über die Hälfte der behandelten Patienten darauf anspricht.
Neben einer Abnahme der Tumormassen oder der Verhinderung eines weiteren Tumorwachstums führt die Therapie auch zu einem sinkenden PSA-Wert.
Die Therapie kann jedoch die Patienten nicht heilen, die Wirkung ist palliativ.
Die Tumorerkrankung schreitet langsamer fort und der Patient hat weniger Schmerzen. Dadurch wird seine Lebensqualität entscheidend verbessert. In Einzelfällen sind kurz nach der Therapie keine Tumorherde mehr nachweisbar.
Eigene Erfahrung, Meine Therapie in Katharinenhospital in Stuttgart, Ablauf
Die Voraussetzung für die Therapie waren vorher erfolgreich durchgeführte PSMA-PET-CT und Nieren Szintigraphie.
Ich war am Dienstag gegen 8 Uhr ins Krankenhaus aufgenommen.
Gegen 11 Uhr wurde mit Flüssigkeitsinfusion angefangen.
Auf Grund einer Speicherung von Lutetium-177 PSMA in den
Speicheldrüsen habe ich 30 Minuten vor und bis zu 4 Stunden nach der Therapie
Kühlpackungen erhalten, mit denen die Speicheldrüsen gekühlt und somit geschützt werden können.
Die Therapie mit Lutetium-177 PSMA erfolgte gegen 12 Uhr und dauerte ca. 15 Minuten.
Um Schäden an den Nieren zu vermindern, wurde weiterhin während und bis in die Nacht Flüssigkeitsinfusionen über die Vene verabreicht.
Ich musste auch am Therapietag und den Folgetagen viel trinken, um die Strahlenbelastung der Nieren und des restlichen Körpers zu verringern.
In den Folgetagen nach der Therapie werden szintigraphische Ganzkörperaufnahmen und Blutentnahme durchgeführt, um die Speicherung von Lutetium-177 in den Tumorzellen und den Abbau der Therapiesubstanz zu kontrollieren.
Erst am Freitag (also nach 4 Tagen) wurde ich entlassen und durfte die Therapiestation verlassen.
Ca. 1 Monat nach der zweiten Lutetium Therapie wurde bei mir erneut PSMA-PET-CT durchgeführt, um den Erfolg der Therapie zu kontrollieren.
Patienteninformationsblatt über Lutetium Lu-177 Therapie: => Lutetium-Therapie-Info
Da nach über einem Jahr mein PSA-Wert hat angefangen wieder zu steigen und in PSMA-PET-CT zeigten sich neue Metastasen und einige alte wuchsen wieder, habe ich mich entschlossen für weiter Behandlung mit der Kombination Lutetium 177 mit Actinium 255 in Heidelberg.
Eigene Erfahrung Lutetium mit Actinium Therapie in Universitätsklinik Heidelberg
Im November 2020 hatte ich in der Nuklearmedizin von Uni-Klinikum Heidelberg die erste Kombitherapie mit Lutetium und Actinium mit folgender Kombination:
Lu177 mit 2 GBq
Ac225 mit 6 MBq.
Vor der Therapie war mein PSA-Wert bei 9 ng/ml, ist schnell gewachsen.
Nach der Therapie PSA-Test am 14. Dezember ergab PSA-Wert von 0,4 ng/ml, meine Leukozyten waren sehr niedrig bei 3,3.
Mein Prostatakrebs Verlauf im Jahr 2020: mein prostatakrebs-2020/
Uni-Klinikum Heidelberg, zweite Kombitherapie mit Lutetium und Actinium mit folgender Kombination in die Vene bei laufendem Tropf rein-gespritzt:
Lu177 mit 4 GBq
Ac225 mit 4 MBq.
also weniger Actinium und mehr Lutetium. Warum? „so hat der Oberarzt entschieden“ war die Antwort.
Am 21.02.2021 PSA Wert unter der Nachweisgrenze
Seit Dezember 2021 steigt mein PSA wieder
Wo wird PSMA Therapie durchgeführt? Kliniken:
Die Therapie wird an verschiedenen Unikliniken erfolgreich angewandt, zum Beispiel an der Uniklinik Köln, Heidelberg, Universitätsklinikum des Saarlandes, Universitätsklinikum Bonn, Zentralkilinik in Bad Berka, Universitätsklinikum Jena, Katharinenhospital Stuttgart.
Therapieablauf in der Zentralklinik Bad Berka
Eigene Erfahrung von einem Patient:.
Die Dauer der stationären Aufnahme beträgt meist fünf Tage; z.B. Anreise sonntags oder montags, Abreise am Donnerstag oder Freitag.
Bevor die eigentliche Therapie durchgeführt wird, erfolgen verschiedene Untersuchungen.
Am Therapietag müssen mindestens 1,5 Liter Flüssigkeit getrunken werden, um die Belastung der Niere so gering wie möglich zu halten (beschleunigte Ausscheidung).
Die Gabe der Therapiesubstanz Lutetium-177 PSMA erfolgt intravenös über eine Armvene und dauert ca. 15 Minuten.
Zur Verringerung der Nierenbelastung werden die Nieren im unmittelbaren Zeitraum vor und nach der Therapie durch Infusionen (z.B. Aminosäuren) geschützt.
Nach Infusion der Therapiesubstanz muss der Patient für 48 Stunden auf der Isotopen-therapie-Station verbleiben (gesetzliche Vorschrift).
Die Kontrolle der Anreicherungsintensivität in den Metastasen sowie Messungen zum Abbau der Therapiesubstanz im übrigen Körper erfolgen in der Regel täglich durch sogenannte szintigraphische Ganzkörperaufnahmen auf der Therapiestation (sowie mittels einer speziellen Tomographie/ Schichtuntersuchung mittels SPECT/CT einer Tumorregion).
Während des stationären Aufenthaltes und in den Tagen danach wird eine erhöhte Flüssigkeitsaufnahme (mind. 1,5 Liter täglich) empfohlen.
Die Therapie wird üblicherweise nach ca. 2 Monaten (6-10 Wochen) wiederholt, vor einem eventuellen dritten Therapiezyklus erfolgt erneut eine PSMA-PET-CT Kontrolluntersuchung.
Kosten für PSMA Therapie
Seit dem 01.01.2016 ist PSMA Therapie im Leistungskatalog der gesetzlichen Krankenkassen verzeichnet und wird oft erstattet, sofern die Voraussetzungen für diese Therapie erfüllt sind.
Ich musste als gesetzlich Versicherte im Katharinenhospital Stuttgart für Lutetium Therapie und in Universität Heidelberg für Lutetium + Actinium Therapie keine Kosten tragen, da ich für die Therapien eine Krankenhauseinweisung (Verordnung von Krankenhausbehandlung) hatte.
Die Kosten, die ich hier vorstelle wurden mir von einem Patient von Klinikum in Heidelberg genannt.
Materialkosten ca. 2.000 EUR
Krankenhauskosten, Unterbringung, Untersuchung: ca. 1.800 EUR
Kosten für 1 Zyklus: ca. 3.800 EUR, für 3 Zyklen: ca. 12.000 EUR
Die genannte Kosten würden nach einem Antrag von der Krankenkasse teilweise übernommen.
Zulassung PSMA Therapie
Die für die Zulassung notwendige Studie wurde bereits Ende 2018 angekündigt: eine multinationale, randomisierte Phase-III-Zulassungsstudie (VISION; NCT03511664). Die Ergebnisse sollen Ende 2021 publiziert werden.
Die bisherige Ergebnisse der Lu PSMA-Studie zeigen hohe Ansprechraten mit geringer Toxizität und Schmerzlinderung.
Bei der Studie sollen Patienten mit einem mCRPC nach Vorbehandlung mit Abirateron und/oder Enzalutamid und nach Docetaxel mit 177Lutetium-PSMA-RLT behandelt werden.
Jede 6-8 Wochen bis zum Ende der Behandlung und jede 3 Monate während langfristiger Nachverfolgung bis zu 24 Monate
Schlagwörter: PSMA Therapie, Lutetium, Actinium, Nebenwirkungen
Mich würde hier in dem Forum interessieren wie man mit den Schmerzen klar kommt. Ich habe im Moment starke Schmerzen in der rechten Hüfte/Steiß, Rücken. Was für Schmerzmittel wären noch wirksam? Ich nehme aber schon Targin 40/20 und Effentora 400.
Gegen die Metastasenschmerzen soll eigentlich die PSMA-Therapie helfen (Lutetium, Aktinium). Manchmal wirkt erst nach 4 Zaklen.
Gegen Schmerzen gibt es sehr viele Starke Medikamente. Stärker als Targin sind zum Beispiel Hydromorphon, Fentanyl.
Ich würde zu einem Schmerztherapeut (Arzt) gehen, da alle Schmerzmittel haben starke Nebenwirkungen.
Dazu, jeder Mensch ist anders und die Verträglichkeit und Wirkung können variieren.
Ich habe mein Wissen über Schmerzmitteln bei Krebs aud folgender Seite beschrieben:
https://krebs-tumoren.de/schmerztherapie-mit-medikamenten/
Hallo, seit Januar 2014 lebe ich mit der Diagnose : kastrationsresitendes Prostatakarzinom. Da war ich 53 Jahre alt.Ich habe nie etwas von der Krankheit bis zu den ischiasschmerzartigen Anfällen im Jahr vor der Diagnose in immer kürzeren Abständen gemerkt. Ich dachte es kommt von der Arbeit. Ich hatte und habe keine Probleme mit dem Wasser lassen, bei mir ist der Tumor nach außen durchgebrochen. Dummerweise ist der Tumur agressiv, Gleason Scquare 4 + 4. Meine Therapie: Firmagon, Xgeva, Prednisolon, nach einem Jahr Xofigo, danach noch Xtandi. Gegen Schmerzen Targin und Durchbruchsschmerzen (die leider schlimmer und häufiger werden) Effentora 400. Mein PSA sank von über 4000 auf 4, aktuell bei 60. Zwischendurch Bestrahlungen betroffener Regionen die schmerzten. PSA sank wieder etwas. Voriges Jahr im Dezember dann Lutetium, habe ich one Probleme gut vertragen, die nächsten 2 Termine wird dann die Kombination von Lutetium und Actinium verabreicht. Meine Fragen: wie gut ist die Verträglichkeit ? , wie groß sind meine Chancen weiterhin relativ beschwerdefrei zu leben bzw. wie hoch könnte die Lebenserwartung sein? Was kann ich gegen die nervenden Schmerzen die wie Ischiasschmerzen von der Wirbelsäule über die Hüfte zum Oberschenkel ziehen tun ? Ich kann manche Tage nicht auf dem Rücken liegen, MRT, CT usw. sind nur mit Schmerzspritzen möglich. Ich habe großen Lebenswillen, interessante Hobbys, neue Freundin, ich meine wenn es nach mir geht noch zwanzig Jahre.
Hallo,
die Kombination Lutetium mit Actinium wirkt viel besser und viel stärker als Lutetium alleine.
Die Verträglichkeit ist ähnlich, aber Actinium greift viel stärker die Speicheldrüsen an.
Ich hatte meine zweite Lu+Ac Therapie am 20 Januar und habe aktuell keine Spucke im Mund.
Hier habe ich mehr über die Therapie und meine Erfahrung geschrieben:
http://prostatakrebs-tipps.de/lutetium-actinium-psma-therapie/.
Lebenserwartung? Nicht daran denken, aber einfach das Leben genießen.
Wir wissen nicht, wie lange wir leben werden und jeder von uns mit Prostatakrebs hat einen eigenen Karzinom.
Positiv denken, Hoffnung haben, das verlängert das Leben enorm.
Gegen die Ischiasschmerzen da müssen Sie die Bauch und Rückenmuskulatur trainieren. Ich würde Ihnen eine orthopädische REHA empfehlen. Ich war auch wegen LWS-Schmerzen (auch Durchbruchschmerzen) für 3 Wochen in REHA und dort habe ich gelernt mich anders zu bewegen (Rückenschule), so dass ich jetzt nur selten Rückenschmerzen habe.
Hilfreich kann auch ein orthopädische Korsett sein, aber anziehen nur für ein paar Stunden. Längeres Tragen ist für die Muskulatur nicht fordernd.
Vielen Dank. Kommt die Spucke wieder? Positiv denken ist richtig, sonst hätte ich es nicht so weit geschafft. Nun ist der Punkt erreicht wo die Schmerzen zunehmen und daher die Therapie. Wenn es dann wieder 2-3 Jahre mir gut geht ist alles okay. Nur ist jetzt die Jahreszeit und die Corona-Maßnahmen nicht gerade förderlich.Wegen Lebenserwartung, das hat andere Gründe. Ins Grab kann mann kein Geld nehmen. Besser ist alles zu verleben aber sinnvoll.
Hallo Jacekw,
ein Cousin meiner Freundin hat Prostatakrebs und erhält Bestrahlung und eine Chemotherapie. Wie hoch ist die Heilungsrate bei der PSMA Therapie?
LG
Stefan
Hallo Stefan,
Bei einer PSMA-Therapie geht es nicht um eine Heilung, sondern um eine Lebensverlängernde Behandlung. Radioaktive Substanzen gelangen an Krebszellen die PSMA Rezeptoren aufweisen und greifen sie an. Bei ca. 60% behandelten Männern sinkt der Psa Wert um mehr als 50%, Metastasen werden verkleinert und teilweise verschwinden.
Ich bin gerade im Krankenhaus wo ich den zweiten Zyklus der Therapie bekomme und bin froh, dass es die Therapie gibt. Sonst gibt es für mich keine Therapie die noch wirken kann.
LG Jacek
Über eine Freundin erhielt ich den Hinweis auf folgenden Artikel über die Lutetium-PSMA-Therapie, der für die meisten von uns sicher wichtig ist. Bitte nachlesen und sich selbst ein Urteil bilden.
http://www.spiegel.de/gesundheit/diagnose/uniklinik-frankfurt-zweifelhafte-psma-therapie-gegen-prostatakrebs-a-1244065.html#ref=nl-spiegeldaily
danke, habe gelesen.
Für mich ist die PSMA-Behandlung bei fortgeschrittenem Prostatakrebs nicht zweifelhaft. Es ist leider so, dass nicht alle Prostatakarzinom-Zellen genug PSMA haben, dass die Behandlung bei allen Männern gut funktionieren kann.
Außerdem, eine PSMA-Therapie ist nur eine Option, die das Leben verlängern kann, heilen wird in den meisten Fällen nicht.
Auch mir wurde letzte Woche von Uni Tübingen eine PSMA-Behandlung empfohlen, nach dem bei PSMA-PET neue Metastasen gefunden wurden.
Für mich ist sehr zweifelhaft, was Spiegel immer wieder schreibt, ohne sich mit dem Thema ausreichend zu beschäftigen und informieren.
Danke für die sehr informativen Berichte.
Ich habe seit 2000 Prostatakrebs, wurde in Heidelberg
bestrahlt und habe dann mit 3 -facher Hormonblockade
(toxische Hepatitis durch Casodex)und intermittierender
Hormonblockade(Enantone)therapiert.Seit 2012 hormonrefraktär.
Seit 2015 (PSA 560) nehme ich XTANDI.Habe Metastasen in der
Wirbelsäule und in den Lymphknoten im Bauch.Ende 2016
Wirbelbruch.Anschließend Bestrahlung der Wirbelsäulen-
metastasen mit Rapid Arc.Seit 2 Wochen wird eine neue Metastase
im Halswirbel bestrahlt. Das PSMA PET in 2016 zeigte,
dass PSMA exprimiert wird. Ist nach all diesen externen Bestrahlungen noch eine Lutetium Therapie sinnvoll?
In jedem Fall ist eine Lutetium Therapie sinnvoll, aber nicht sofort.
Ich würde zuerst die Bestrahlung fertig machen und schauen (ca. 2 Monate danach) ob PSA-Wert sinkt.
Dann eine neue PSMA-PET machen.
Eigentlich bei Metastasen solle man 1 bis 2 mal im Jahr eine bildgebende Untersuchung machen.
Vielleicht wäre noch eine Therapie mit Xofigo möglich, gegen die Knochenmetasasen (bei kleinen Lymphknoten Metastasen ist möglich).
Da Xtandi nicht mehr wirkt, vielleicht mit Zytiga +Prednisolon probieren.
Hallo jacekw
Danke für die schnelle Antwort,die
ich erst heute lese.Die Bestrahlung
von HWK5 hat den Tumor auf die Hälfte
verkleinert (MRT nach 6Wochen) und die
Schmerzen beseitigt.Anfang August
wurden Metastasen im Acetabulum Und
Im BWK 6 u.7 festgestellt.Sie wurden
mit 40Gray bestrahlt.Leider brach
Anfang September der rechte humerus.
Er wurde erfolgreich fixiert und
mit 30 Gray bestrahlt. Leider kann
ich nur unter Schmerzen gehen.(Belastungsschmerz der linken Hüfte
trotz BESTRAHLUNG.)PSA ist inzwischen
auf 1000 gestiegen.Seit 28.9.Nehme
ich Zytiga(250 mg mit Verstärkung)
Kann die Hüftbestrahlung (Ende am
17.9)die Schmerzen noch lindern?
Herzliche Grüße Gerd
Hallo Gerd, es tut mir leid es zu lesen, wie sich die Erkrankung bei Dir breit macht.
Habe mir überlegt, was Du noch machen kannst.
Vielleicht mit Xofigo versuchen, oder PSMA-Therapie.
Gegen Schmerzen sind da nur die Opiate (eventuell auch Methadon?) hilfreich.
Es tut mir leid, dass ich Dir nicht viel helfen kann.
Ich habe heute erfahren, dass mein PSA trotz Hormonblockade und Bestrahlungen (Zytiga vertrage ich nicht) sich in den letzten 6 Wochen verdoppelt hat.
Ich bin aktuell in einer Anthroposophischen Klinik in Öschelbronn. Ich lerne hier die Hoffnung nicht zu verlieren. Wir haben sehr starke Selbstheilungskräfte in uns. Manchmal verschwinden „unheilbare“ Tumore von alleine mit der Unterstützung der positiven Gedanken.
Herzliche Grüße, Jacek
Hallo jacekw,Danke für Deine Antwort.Ich habe vor 2 Wochen
mit Zytiga angefangen.Nur 1/2 Dosis und Öl zur Verstärkung.
Ich muss die Leberwerte alle 2 Wochen überprüfen
wg Vorschädigung. Prednison habe ich gegen 0,5mg Dexa
getauscht. Dir wünsche ich viele positive Gedanken
In Öschelbronn,Dein PSA Anstieg ist vielleicht ein bounce
nach Bestrahlung?? Viel Gluck.Herzliche Grüße Gerd
Hallo, nachdem ich in unserem Stadtkrankenhaus austherapiert war, habe ich nach Kampf mit der Krankenkasse den Weg nach Heidelberg bestritten, anfang August mit grossen Schmerzen und noch zwei drittel meiner Leber (Metastasen) und noch vielen Metasten im gesamten Knochenskelett ging ich nach Heidelberg zur PSMA Liganden Therapie, Ich war im August 2017 3 Tage dort zur ersten Behandlung Untersuchung Knochencynti ect. am 2 Tag bekam ich dan das Therapeutikum eine Spritze in die Kanüle 1Minute das wars, nach 2 Tagen konnte ich das Klinikum verlassen.Nach ca.1 Woche fing es an mir besser zu gehen Schmerzen wurden weniger keine Nebenwirkung,mittlerweile war ich jetzt ende November das dritte mal dort und muss erst wieder mitte Januar hin mit einem verbessertem Therapeutikum. Was soll soll ich sagen mir geht es wieder richtig gut, mein PSA Wert ist von 67 auf 1,7 gesunken Metastasen im Körper sind teilweise nicht mehr zu sehen und oder sind viel kleiner geworden.Nutzt den Fortschritt der Medizin, habe mich mit ein paar Patienten Unerhalten, einer war sogar von Übersee extra nach Heidelberg auch in seiner Heimat austeraphiert, kamm mit PSA 1200 hatte im letzten Blutuntersuchung PSA von 56 und kaum noch Schmerzen.Keine Ahnung wie lange das anhalten wird aber ich werde die geschenkte Zeit geniesen
LG
an alle hier, und schöne und Lebendige Feiertage
Hallo Kyra,
gratuliere für diesen Erfolg. Es freut mich sehr, dass die Therapie bei Dir so gut anschlägt.
Genieße jetzt die Weihnachtszeit, Alles Gute
Jacek
Hallo Kyra und jacekw
ich freue mich über die genaue Ausführung der Therapie. Ich habe eine Frage. Welchen Gleason Score hattest oder hast du bei der Erstdiagnose gehabt? Ich frage weil mein Vater die 9 hat und Metastasen in Oberschenkel und Beckenknocken und Lymphknoten hat. CyberKnife wurde erst vor ca 3 Wochen an den metastasen durchgeführt. Nun hat er Schmerzen unter der Hormonbehandlung mit Xtanti und überleget diese PSMA Therapie zu machen. Sein PSA steht bei ca 0,73 und ist seit 2 Wochen von 0,52 auf diesen Wert gestiegen.
ich hatte Gleason Score 8.
Vielleicht ist eine Behandlung mit Xofigo möglich (Lymphknotenmetastasen bis 3 cm sind erlaubt)
Die Behandlung haben die Ärzte schon ausgeschlossen, da im Bauchraum neue Metastasen in den Lymphen sitzen. Die Schmerzen in der Hüfte machen ihm sehr zu schaffen. Man sagt ja die Wirkung nach CyberKnife dauert eine Zeit bis es endgültig wirkt. Was sagst du zu der neuen PSMA Liganden Therapie?! Sein Urologe meinte man müsse wenn der PSA über 1 steigt wieder eine Chemo machen. Ist es denn bedenklich das der PSA so langsam steigt unter Gabe von Xtandi oder eher normal? Habt ihr da Erfahrung?
Wie geht es dir eigentlich jacekw?
Hallo Gaschi,
wenn bei der Xtandi-Behandlung der PSA-Wert steigt, bedeutet das, dass die Behandlung nicht vollständig anschlägt.
ich würde so machen, wie der Urologe empfehlt: wenn der PSA-Wert weiter steigt, mit Chemotherapie wieder anfangen, aber nicht mehr mit Docetaxel, sondern mit Cabazitaxel. Wirkt auch mit niedriger Dosierung (weniger Nebenwirkungen).
Erst danach würde ich mit PSMA Liganden Therapie machen.
Wie geht es mir? Es geht. Habe in April eine Bestrahlung einer Metastase in der Wirbelsäule gehabt, gleich danach Innenohr OP.
Medikament Zytiga vertrage ich nicht, mit Xtandi habe ich noch nicht angefangen. Diese Woche werde ich PSA-Test machen und sehe, ob die Bestrahlung was gebracht hat.
Ich bin oft sehr Müde, depressiv, aber ich kämpfe weiter.
Nächste Woche fahre ich wieder für eine Woche in die Klinik Öschelbronn: Hyperthermie und andere anthroposophische Behandlungen.
Gruß, Jacek
Hallo allerseits, insbesondere den Medizinern hier –
mein kürzliches Gallium – PSA- Pet Ct ergab nach 3- jähriger Einnahme von Xtandi und anfänglich geradezu sensationellen PSA – Abfall von 80 auf 6, erneut eine Zunahme der Lymph – Mestastasen im hinteren Bauchfell, hoch bis zum Brustraum, große Strukturen 5 mm bis 3,5 cm. PSA jetzt 37.
Knochen, Lunge und Hirn M.-frei, wie man mir sagte.
In der Vorgeschichte wurde 2005 operiert und 2006 bestrahlt.
2011 erfolgte eine Lymph-OP, in der aber nicht alle M. beseitigt werden konnten.
Mein Urologe empfahl jetzt wahlweise eine Chemotherapie, vor der ich einen wahren Horror habe, bzw. eine Lutetium – Therapie.
Ich lese, die zur Behandlung empfohlene Klinik arbeitet mit der
Substanz Lutetium 177 PSMA.
An anderer Srelle lese ich, dass Lutetium 131Iod noch empfehlenswerter sei, da die Strahlung nur 1,5 mm weit reiche.
Außerdem: Micro-Metastasen könnten ohnehin nur erfolgreich behandelt werden, wenn der PSMA-Ligand mit einem Alphastrahler wie Radium verbunden wird.
Solange mit Betastrahlen gearbeitet würde muss mit Nebenwirkungen gerechnet werden, die die Wiederholbarkeit ein-
schränken oder wenig sinnvoll machen.
Hinsichtlich der Strahlenbelastung geistern astronomische Horrorzahlen über Infoseiten, wie – 45 Gray entsprechen ca. 45000 Röntgenaufnahmen.
Mit der empfohlenen Klinik zu sprechen, erscheint wenig sinnvoll.
Also ist guter Rat teuer.
Im voraus herzlichen Dank
Es kann sein, dass nach Xtandi noch Zytiga wirken kann.
Ich habe vor kurzem gehört, dass nach einer Chemotherapie Zytiga und Xtandi wieder wirken können.
Alpharadin (Radium Alphastrahler) ist vorgesehen nur zur Behandlung von Metastasen in den Knochen.
PSMA Therapie mit Actinium-225 ( ein α-Strahler) verursacht mehr Nebenwirkungen als Lutetium-177 (ein ß-Strahler).
Nebenwirkungen von Chemotherapie werden kleiner, wenn sie in 2-Wochen-Zyklus (mit niedrigerer Dosis) durchgeführt wird. Standard ist ein 3-Wochen-Zyklus.
Wäre für Ihre Anrwort besonders dankbar – Dr. med. xxx.xxx
Ob Ihre hier einsehbaren, früheren Kommentare auf mich anwendbar sind, kann ich leider nicht beurteilen.
Wenn der Seitenbetreiber Ihnen meine e-mail-Adresse zur Verfügung stellt – von mir aus sehr gerne.
Danke im voraus.
Ch.
Hallo,
„Dr. med. xxx.xxx“ hat schon seit langem kein Kontakt mit mir aufgenommen, so glaube ich nicht, dass er auf Ihre Frage antworten wird.
LG Jacek W.
Hallo,
mein Vater ist 80Jahre, Erstdiagnose 2004 PC( gleason 4+4, PSA :35ng/ml, 3 fache Hormontherapie+perkutaner Betrahlung der Prostata.Befall lediglich innerhalb der P-Kapsel)
Seit 2016 PSA -Werte über 10ng/ml, Kastrationsrezistents, letzter PSA-Wert:18,68ng/ml.07/2017 und Mehrere Knochenmetastasen.
Sein Urologe empfield mit Xtandi weiterzu machen. Aber die Nebenwirkungen der jahrelangen Hormontherapie macht Ihm durch Vergesslichkeit, Schwindel, starke Depressionen, Kraftlosigkeit stark zu schaffen.
Könnte die Therapie mit Lutetium-177 PSMA für meinen Vater in frage kommen(Alterswegen?) Welchen Anteil würde die GKV übernehmen?
Vielen Dank in voraus!
Samil
PSMA-Therapie hat starke Nebenwirkungen, wird nur als Studie durchgeführt, ich würde sie Ihrem Vatter nicht empfehlen.
Ich würde mit dem Urologen sprechen, ob er nicht Zytiga verschreiben kann. Auch Xtandi kann man nehmen und im Fall starken Nebenwirkungen abbrechen.
Andere Alternativen sehe ich führ Ihren Vatter derzeit nicht.
VIELE Grüße, Jacek W.
Zitat:“PSMA-Therapie hat starke Nebenwirkungen, wird nur als Studie durchgeführt“
Das stimmt so nicht bzw. nicht mehr. Nebenwirkungen, wenn überhaupt, sind eher harmlos und die Therapie ist inzwischen, zumindest an den meisten Unikliniken, etabliert
Haben Sie eine antihormonelle Therapie? Und ist der PSA darunter im Laufe des Jahres drastisch gefallen? Wurde die PSMA-PET/CT bei fallendem PSA durchgeführt? Dann kann sie unauffällig („PSMA-negativ“) ausfallen.
Ich habe einen Fall, bei dem die Metastasen nach mehreren Monaten antihormoneller Therapie in der PSMA-PET/CT komplett verschwunden sind. Der Patient hat aber eine intermittierende Therapie und in der Therapiepause ist der PSA jetzt auf 16 ng/ml angestiegen und die Metastasen sind nun zum Teil wieder sichtbar geworden.
Eine andere Möglichkeit: Handelt es sich um ein neuroendokrin differenziertes Prostatakarzinom? Dann könnte das deshalb PSMA-negativ sein, müsste aber Somatostatinrezeptoren (SSTR) haben. Dann könnte man das mit einer Gallium-68-DOTATATE-PET/CT untersuchen und im Falle einer deutlichen SSTR-Bildung sogar gut mir einer Lutetium-177-DOTATATE-Therapie behandeln (also ähnlich wie ein PSMA-positives Prostatakarzinom mit Lutetium-177-PSMA-617 behandelt wird).
Ein PSA-Anstieg kann mindestens 4 verschiedene Gründe haben:
1.) Absetzen der antihormonellen Therapie, um eine möglichst hohe PSA- und PSMA-Expression und damit einem möglichst guten Behandlungserfolg zu erzielen. Wie hat sich der PSA nach der vierten PSMA-Therapie entwickelt? Solange der Testosteronwert steigt, kann der PSA auch noch steigen. Vielleicht ist der PSA nun aber auch gefallen, weil die 4. PSMA-Therapie gut wirken konnte. Das wäre dann sehr erfreulich.
Ich habe gerade erlebt, dass nach Absetzen der antihormonellen Therapie bei steigendem Testosteron der PSA 01/2016 bis 756 ng/ml anstieg (was alle Kollegen sehr erschreckte). Nach der 3. PSMA-Therapie fiel der PSA dann aber in 4 Wochen auf 690 ng/ml und nach weiteren 3 Wochen sogar auf 526 ng/ml! Jetzt soll die 4. PSMA-Therapie erfolgen. Der Mann hat weiterhin keine antihormonelle Therapie mehr. Es geht ihm gut. Er ist schmerzfrei, hat keine Nebenwirkungen der antihormonellen Therapie mehr und arbeitet wieder.
2.) Die abnehmende Wirkung einer antihormonellen Therapie ist der Grund für den Beginn einer Radium-223-Therapie oder PSMA-Therapie. Man nennt das wie Sie wissen „hormonrefraktär“. Das ist aber kein plötzliches Ereignis, sondern ein langsamer Prozess. Also kann trotz fortgesetzter antihormoneller Therapie der PSA-Wert weiter steigen, weil langsam immer noch mehr Metastasen hormonresistent werden, die erst dann genügend PSMA bilden und auf eine PSMA-Therapie ansprechen.
3.) Falls die PSMA-Bildung der Tumorzellen ungenügend ist, kann nicht genug Lutetium-177-PSMA-617 an den Metastasen binden und diese werden dann nicht ausreichend intensiv bestrahlt. Dann kann es wegen der unzureichenden Wirkung der PSMA-Therapie zu einer Zunahme von Metastasen kommen und der PSA-Wert kann sogar steigen.
Nach meiner Erfahrung wird die Aktivität der Tumorzellen und damit die PSA- und PSMA-Bildung durch eine gleichzeitige antihormonelle Therapie gehemmt. Das kann meines Erachtens zum Versagen der PSMA-Therapie führen. Ich empfehle daher, die antihormonelle Therapie vor einer PSMA-Therapie abzusetzen, damit die Metastasen viel PSA und PSMA bilden und die Therapie möglichst gut wirken kann. Der PSA-Wert ist dann nicht mehr künstlich geschönt, sondern zeigt die wahre Realität und ein vermutlich umso besseres Ansprechen auf die PSMA-Therapie.
Die Meinungen gehen hierüber aber sehr auseinander. Leider gibt es hierzu bisher keine Studienergebnisse, sondern nur Fallbeispiele, die meine Vermutung stützen.
4.) Es gibt unterschiedliche Messverfahren. Die Ergebnisse können nach Literaturangaben um 20 % schwanken. Man sollte daher gegebenenfalls fragen, welche Methode der Urologe angewendet hat und welche Methode die Klinik anwendet.
Hallo Herr Dr. XXXX,
inwiweit ist diesr Kommentar auf meine Frage vom 16.11.20917
anwend- und übersetzbar.
Alles ja nicht ganz so einfach für Laien. 🙂
Dank im voraus
Charlie